人体肠道菌群从婴儿刚出生时就开始建立,随着婴儿的成长,肠道菌群逐渐演变,其过程较为复杂。婴儿刚出生时肠道内无微生物,在接触母体、周围环境以及脐带结扎的过程中逐渐接触到微生物,微生物开始在肠道中定殖。[1]
0-3岁是宝宝成长的关键时期,此时肠胃发育是否正常将直接影响宝宝的健康生长。婴幼儿肠胃极其脆弱,许多表面看起来毫不相关的疾病,很多也是源自肠胃问题。所以婴幼儿肠道菌群的建立至关重要,安全性成为最需要关注的点,因此卫健委从2011年开始建立批准《可用于婴幼儿食品的菌种名单》,后续逐渐增加了新食品原料菌株可用于婴幼儿食品。2022年8月25日国家卫生健康委关于《可用于食品的菌种名单》和《可用于婴幼儿食品的菌种名单》更新的公告 (2022年 第4号),公告对菌种名单进行了更新。对名单中涉及菌种分类和命名调整的,设置2年过渡期。本文整理了卫健委批准的8株列入《可用于婴幼儿食品的菌种名单》与7株可用于婴幼儿食品的新食品原料与菌株的介绍并附了合规依据。

嗜酸乳杆菌NCFM
嗜酸乳杆菌NCFM属于乳杆菌科,乳杆菌属,能分解糖类生成L-乳酸,为上世纪70年代早期从北卡罗来纳州立大学从人体粪便中分离出来的菌株。嗜酸乳杆菌NCFM已列入美国一般公认安全(GRAS)名单,被用于多种食品中,包括婴幼儿配方食品;已入欧洲食品安全局资格认定(QPS)名单的推荐生物制剂列表中,并列入国际乳品联合会公报(Bulletin of the IDF 455/2012)的“在发酵食品中有技术必要性的微生物品种目录”。国外开展的多项临床研究证明,该菌株用于1岁以下婴儿具有较好的食用安全性。
2011年原中国卫生部(现中华人民共和国国家卫生健康委员会)已将嗜酸乳杆菌NCFM列入《可用于婴幼儿食品的菌种名单》,限定其仅用于1岁以上幼儿食品。2021年2月18日国家食品安全风险评估中心发布《新食品原料嗜酸乳杆菌NCFM公开征求意见》本次申请扩大用于1岁以下婴儿食品。
动物双歧杆菌乳亚种Bb-12
动物双歧杆菌乳亚种Bb-12自1985年以来在世界范围内被用作食品和膳食补充剂的成分。超过315种科学出版物对其进行了描述,并得到了超过190项临床研究的支持,是拥有大量公开科学研究及临床数据支持的益生菌菌株。动物双歧杆菌乳亚种Bb-12菌株已获得欧洲食品安全局(EFSA)授予的“安全资格认定”(QPS,Qualified Presumption of Safety),美国食品药品监督管理局 (FDA, Food And Drug Administration) 也已将BB?-12双歧杆菌菌株列为“一般公认安全物质”(GRAS, Generally Recognized as Safe)[2]。
2011年11月原中国卫生部(现中华人民共和国国家卫生健康委员会)正式批准用于婴幼儿食品。2022年8月25日国家卫生健康委关于《可用于食品的菌种名单》和《可用于婴幼儿食品的菌种名单》更新的公告 (2022年 第4号),将原动物双歧杆菌Bb-12名称更新为动物双歧杆菌乳亚种Bb-12。
动物双歧杆菌乳亚种HN019
动物双歧杆菌乳亚种HN019菌株是一种革兰氏阳性、厌氧杆状细菌,最初是从新西兰酸奶源分离出来的。动物双歧杆菌乳亚种HN019的食品,被日本政府的消费者厅批准为含健康声称的食品,是日本首个允许食品生产商在产品上进行健康声称的乳双歧杆菌菌株。动物双歧杆菌乳亚种HN019获得了欧盟食品安全委员会资格认定(QPS)推荐的生物制剂列表、美国食品药品监督管理局 (FDA, Food And Drug Administration) 也已将动物双歧杆菌乳亚种HN019菌株列为“一般公认安全物质”(GRAS, Generally Recognized as Safe),2011年11月原中国卫生部(现中华人民共和国国家卫生健康委员会)正式批准用于婴幼儿食品。
2022年8月25日国家卫生健康委关于《可用于食品的菌种名单》和《可用于婴幼儿食品的菌种名单》更新的公告 (2022年 第4号),将原乳双歧杆菌HN019名称更新为动物双歧杆菌乳亚种HN019。
动物双歧杆菌乳亚种Bi-07
动物双歧杆菌乳亚种 Bi-07来源于人体,能在牛奶中生长。革兰氏阳性、厌氧、不产芽孢的多型性杆菌,体外研究表明,动物双歧杆菌乳亚种 Bi-07可以抵抗低PH的条件(在PH3含1%胃蛋白酶的盐酸溶液中37℃培养1小时,存活率达90%以上),并可以在胆盐存在的环境下存活(含0.3胆盐的培养基培养,存活率大于90%)。
动物双歧杆菌乳亚种 Bi-07被列入欧盟食品安全委员会资格认定(QPS)推荐的生物制剂列表、国际乳业联盟(IDF)“具有在食品中安全使用记录史的微生物清单”、美国食品药品监督管理局 (FDA, Food And Drug Administration)列为“一般公认安全物质”(GRAS, Generally Recognized as Safe)。
2011年11月原中国卫生部(现中华人民共和国国家卫生健康委员会)正式批准用于婴幼儿食品。2022年8月25日国家卫生健康委关于《可用于食品的菌种名单》和《可用于婴幼儿食品的菌种名单》更新的公告 (2022年 第4号),将原乳双歧杆菌Bi-07名称更新为动物双歧杆菌乳亚种Bi-07。
鼠李糖乳酪杆菌GG
鼠李糖乳酪杆菌GG是从健康人体肠道中分离得来,自1990年以来鼠李糖乳酪杆菌GG菌株在全世界范围内被用作食品原料和膳食补充剂的成分。已有超过250篇临床研究文献对其进行了论述,其中涵盖新生儿、早产儿、儿童、孕妇、成年人、老年人等人群的不同健康领域。[3]鼠李糖乳酪杆菌GG已获得欧洲食品安全局(EFSA)授予的“安全资格认定”(QPS,Qualified Presumption of Safety) ,被美国食品药品监督管理局 (FDA, Food And Drug Administration)列为“一般公认安全物质”(GRAS, Generally Recognized as Safe)。
2011年11月原中国卫生部(现中华人民共和国国家卫生健康委员会)正式批准用于婴幼儿食品。2022年8月25日国家卫生健康委关于《可用于食品的菌种名单》和《可用于婴幼儿食品的菌种名单》更新的公告 (2022年 第4号),将原鼠李糖乳杆菌LGG名称更新为鼠李糖乳酪杆菌GG。
鼠李糖乳酪杆菌HN001
鼠李糖乳酪杆菌HN001最初从新西兰生产的切达干酪中分离出来,它存在于乳制品中并拥有悠久的食用历史。在新西兰乳业研究所筛选出的200个菌株中,HN001被鉴定为潜在的益生菌菌株,用于进一步的动物和人体研究。该菌株被保藏于澳大利亚政府分析实验室(AGAL)。
鼠李糖乳酪杆菌HN001已列入欧盟食品安全委员会资格认定(QPS)推荐的生物制剂列表、美国食品药品监督管理局 (FDA, Food And Drug Administration)列为“一般公认安全物质”(GRAS, Generally Recognized as Safe)。2011年11月原中国卫生部(现中华人民共和国国家卫生健康委员会)正式列入《可用于婴幼儿食品的菌种名单》。
2022年8月25日国家卫生健康委关于《可用于食品的菌种名单》和《可用于婴幼儿食品的菌种名单》更新的公告 (2022年 第4号),将原鼠李糖乳杆菌HN001名称更新为鼠李糖乳酪杆菌HN001。
罗伊氏粘液乳杆菌DSM17938
罗伊氏粘液乳杆菌(Lactobacillus reuteri ,L reuteri)DSM 17938是罗伊氏乳杆菌ATCC 55730的子代菌株,该菌呈棒状,无芽孢,革兰染色呈阳性。最适合生长温度为30-40℃,适宜PH为5.5-6.2。于1990年由Ivan Casas博士从一位生活在安第斯山脉(位于秘鲁)的妇女母乳中分离出来。《世界胃肠病学组织全球指南(2017更新版)》建议婴儿服用罗伊氏粘液乳杆菌DSM 17938作为预防婴儿肠绞痛的措施。
2014年6月,原卫计委(现中华人民共和国国家卫生健康委员会)批准罗伊氏粘液乳杆菌DSM 17938为新食品原料批准可用于婴幼儿食品[4]。2022年8月25日国家卫生健康委关于《可用于食品的菌种名单》和《可用于婴幼儿食品的菌种名单》更新的公告 (2022年 第4号),将原罗伊氏乳杆菌DSM17938名称更新为罗伊氏粘液乳杆菌DSM 17938。
发酵粘液乳杆菌CECT5716
发酵粘液乳杆菌CECT 5716(Lactobacillus fermentum) 属于乳杆菌属。该菌种已列入欧盟安全资格认定(QPS)推荐的生物制剂列表中,并列入国际乳业联盟(IDF)“具有在食品中安全使用记录史的微生物清单”。2011年发酵乳杆菌列入我国《可用于食品的菌种名单》。发酵粘液乳杆菌CECT 5716分离自健康母乳,经接种、发酵培养、浓缩、冷冻干燥制得。该菌种已通过美国食品药品监督管理局的GRAS(一般认为安全的物质)认定,可用于婴幼儿配方粉。含有发酵粘液乳杆菌CECT 5716的婴幼儿配方粉在欧洲和亚洲等多个国家(地区)均有销售。[5]
2016年6月,原卫计委(现中华人民共和国国家卫生健康委员会)批准发酵粘液乳杆菌CECT 5716列入《可用于婴幼儿食品的菌种名单》批准可用于婴幼儿食品。2022年8月25日国家卫生健康委关于《可用于食品的菌种名单》和《可用于婴幼儿食品的菌种名单》更新的公告 (2022年 第4号),将原发酵乳杆菌CECT5716名称更新为发酵粘液乳杆菌CECT5716。
短双歧杆菌M-16V
短双歧杆菌M-16V(Bifidobacterium breve) 属于双歧杆菌属。该菌种已列入欧盟安全资格认定(QPS)推荐的生物制剂列表中,并列入国际乳业联盟(IDF)“具有在食品中安全使用记录史的微生物清单”。2011年短双歧杆菌列入我国《可用于食品的菌种名单》。短双歧杆菌M-16V分离自健康婴儿肠道内,经接种、发酵培养、浓缩、冷冻干燥制得。该菌种已通过美国食品药品监督管理局的GRAS(一般认为安全的物质)认定,可用于婴幼儿配方粉。含有短双歧杆菌M-16V的婴幼儿配方粉在澳大利亚、新西兰和亚洲等多个国家(地区)均有销售。[5]
2016年6月,原卫计委(现中华人民共和国国家卫生健康委员会)批准短双歧杆菌M-16V列入《可用于婴幼儿食品的菌种名单》,批准可用于婴幼儿食品。
瑞士乳杆菌R0052、长双歧杆菌婴儿亚种R0033和两歧双歧杆菌R0071
2010年瑞士乳杆菌、婴儿双歧杆菌和两歧双歧杆菌已列入我国《可用于食品的菌种名单》。瑞士乳杆菌R0052(Lactobacillus?helveticus?R0052)从乳制品中分离得到,长双歧杆菌婴儿亚种 R0033(Bifidobacterium longum subsp infantis R0033)从婴儿肠道分离得到,两歧双歧杆菌R0071(Bifidobacterium?bifidum?R0071)从成人肠道分离得到。3种菌株粉的性状均为米色颗粒状粉末。瑞士乳杆菌R0052、长双歧杆菌婴儿亚种 R0033和两歧双歧杆菌R0071已通过美国食品药品管理局认证为一般认为安全(GRAS)物质。含有这3种菌株的产品已在加拿大、波兰、澳大利亚被批准用于婴幼儿。国内外开展的多项婴幼儿临床研究证明,该3种菌株具有较好的食用安全性,且耐受性良好。[6]
2020年6月,中华人民共和国国家卫生健康委员会批准瑞士乳杆菌R0052、长双歧杆菌婴儿亚种 R0033和两歧双歧杆菌R0071为新食品原料,批准可用于婴幼儿食品。2022年8月25日国家卫生健康委关于《可用于食品的菌种名单》和《可用于婴幼儿食品的菌种名单》更新的公告 (2022年 第4号),将原婴儿双歧杆菌R0033名称更新为长双歧杆菌婴儿亚种R0033。
鼠李糖乳酪杆菌MP108
鼠李糖乳酪杆菌MP108(Lactobacillus?rhamnosus?MP108)从健康幼儿肠道分离得到,MP108也是目前全球唯一一株分离自中国宝宝健康肠道的婴幼儿菌株,菌粉性状为白色至微棕色粉末。含有该菌株的产品已在澳大利亚生产并上市,可用于婴幼儿食品。国内外开展的多项婴幼儿临床研究证明,该菌株具有较好的食用安全性。[7]
2021年4月,中华人民共和国国家卫生健康委员会批准鼠李糖乳酪杆菌MP108为新食品原料,批准可用于婴幼儿食品。2022年8月25日国家卫生健康委关于《可用于食品的菌种名单》和《可用于婴幼儿食品的菌种名单》更新的公告 (2022年 第4号),将原鼠李糖乳杆菌MP108名称更新为鼠李糖乳酪杆菌MP108。
长双歧杆菌长亚种BB536
长双歧杆菌长亚种(原名称为“长双歧杆菌”)已被列入我国《可用于食品的菌种名单》,也已列入欧洲食品安全局资格认定(QPS)名单的推荐生物制剂列表以及国际乳品联合会公报(Bulletin?of?the?IDF?455/2012)的“在发酵食品中有技术必要性的微生物品种目录”。长双歧杆菌长亚种BB536(Bifidobacterium longum subsp.?longumBB536)从健康婴儿肠道中分离得到,该菌株已在美国、日本被批准用于婴幼儿食品。国内外开展的多项婴幼儿临床研究证明,该菌株具有较好的食用安全性。[8]
2022年5月13日卫健委批准长双歧杆菌长亚种BB536为可用于婴幼儿食品的菌种的新食品原料。
长双歧杆菌婴儿亚种M-63
长双歧杆菌婴儿亚种(原名称为“婴儿双歧杆菌”)已被列入我国《可用于食品的菌种名单》,也已列入欧洲食品安全局资格认定(QPS)名单的推荐微生物列表。[9]长双歧杆菌婴儿亚种M-63(Bifidobacterium?longum?subsp.infantis?M-63)1963年从健康婴儿肠道中分离得到。2022 年,M-63 被美国食品和药物管理局(FDA)认定为GRAS,可用于婴儿配方奶粉和普通食品(GRN 编号,1003)[10]。
2024年8月5日卫健委批准长双歧杆菌婴儿亚种M-63批准列入《可用于婴幼儿食品的菌种名单》。
附:15株国内婴幼儿食品可用菌株法规依据
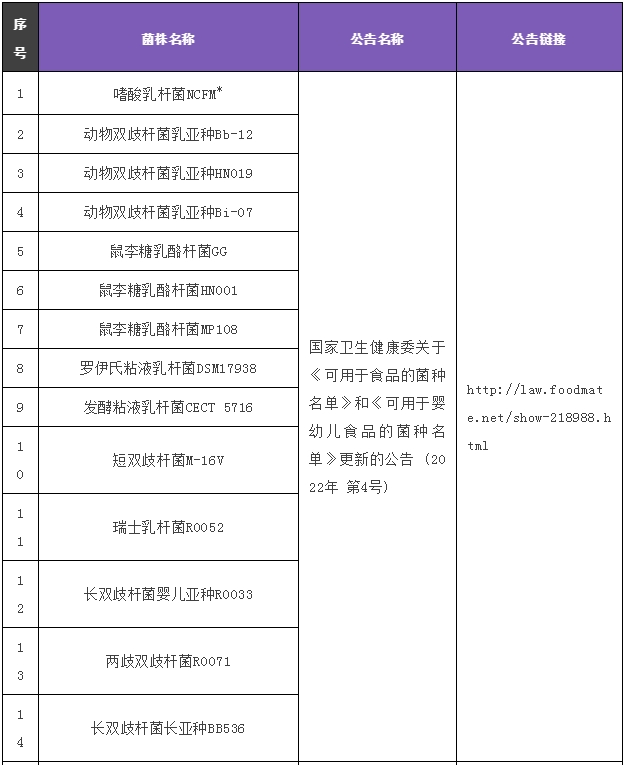

注:带“*”为仅限用于1岁以上幼儿的食品。
名单名称根据:国家卫生健康委关于《可用于食品的菌种名单》和《可用于婴幼儿食品的菌种名单》更新的公告 (2022年 第4号)已更新调整。
参考资料:
[1]王瑞. 陕西不同月龄婴幼儿肠道菌群多样性及优势菌种群研究[D]. 西北农林科技大学.
[2]BB-12™双歧杆菌菌株- 一株全球广泛记载的益生菌菌株—科汉森
[3]LGG®鼠李糖乳杆菌菌株- 一株全球充分验证的益生菌菌株—科汉森
[4]关于公布可用于婴幼儿食品的菌种名单的公告(卫生部公告2011年第29号)—卫健委
[5]解读《关于发酵粘液乳杆菌CECT 5716等3个菌种的公告》—卫健委
[6]关于批准塔格糖等6种新食品原料的公告(2014年第10号)—卫健委
[7]解读《关于β-1,3/α-1,3-葡聚糖等6种“三新食品”的公告》(2021年第5号)-卫健委
[8]解读《关于莱茵衣藻等36种“三新食品”的公告》(2022年第2号)—卫健委
[9]解读《关于阿拉伯木聚糖等8种“三新食品”的公告》(2024年 第3号)—卫健委
[10]探索HMO新时代的益生菌:长双歧杆菌婴儿亚种M-63对婴幼儿健康的益处—森永乳业
来源:食品伙伴网食品研发创新服务中心,图片来源:创客贴会员。
提醒:文章仅供参考,如有不当,欢迎留言指正和交流。且读者不应该在缺乏具体的专业建议的情况下,擅自根据文章内容采取行动,因此导致的损失,本运营方不负责。如文章涉及侵权或不愿我平台发布,请联系处理。









